2022年7月21日,受上海科技大学生物医学工程学院 (上科大生医工学院) 聚焦超声转化研究实验室主任程冰冰教授邀请,美国弗吉尼亚大学生物医学工程学院 Lawrence R. Quarles 冠名讲席教授 Richard J. Price 做客上科大生医工线上学术讲座,为师生带来了题为“Image-Guided Drug and Gene Delivery with Focused Ultrasound”的学术报告,讲座由程冰冰教授主持。
Price 教授是美国弗吉尼亚大学生物医学工程学院 Lawrence R. Quarles 冠名讲席教授,同时担任弗吉尼亚大学聚焦超声癌症免疫治疗中心的联合主任。他从事聚焦超声靶向药物和基因递送的研究已有20余年,是最早发现超声结合微泡造影剂能够打开内皮细胞屏障,从而实现透过血脑屏障的靶向纳米药物递送的科学家之一。近期他的研究方向聚焦在如何利用聚焦超声治疗浸润性胶质瘤和脑转移瘤,以及逆转帕金森病的神经变性。Price 教授在聚焦超声与化疗和免疫治疗协同增效方面的研究,已经成功进入癌症治疗的多个临床试验 (NCT04796220, NCT03237572和NCT04116320) 。
Price 教授首先简要地介绍了聚焦超声 (Focused Ultrasound, FUS)。聚焦超声可以将超声波能量无创地集中到一个椭圆形焦点体积内。与超声成像 (如 B 超) 为代表的诊断超声不同,FUS 作为治疗超声,是一个利用热效应或机械效应治疗疾病的独特工具。本次讲座 Price 教授讲述了 FUS 带来的热效应和机械效应及其生物医学应用。
讲座大纲
Price 教授以凸透镜聚焦阳光点燃树叶为例子,引入聚焦超声的热消融应用 (T-FUS) :将超声聚焦至一个长约 2-4mm、宽约 1-2mm 的体积内并持续施加数分钟的高强度超声辐照后,会使焦点区域产生高温。如果该焦点区域在肿瘤内,通过使肿瘤产生区域凝固性坏死,进而杀死肿瘤。
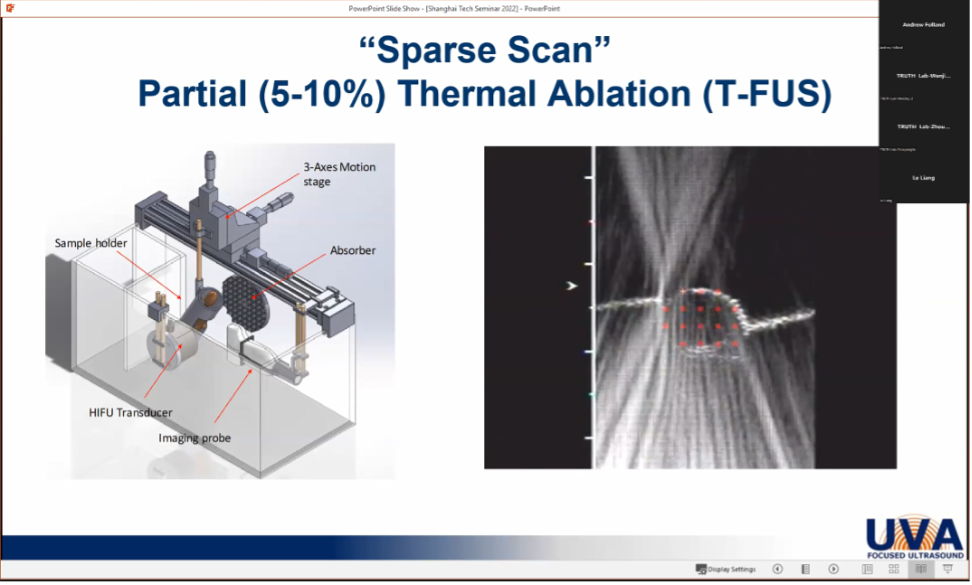
T-FUS 系统示意图
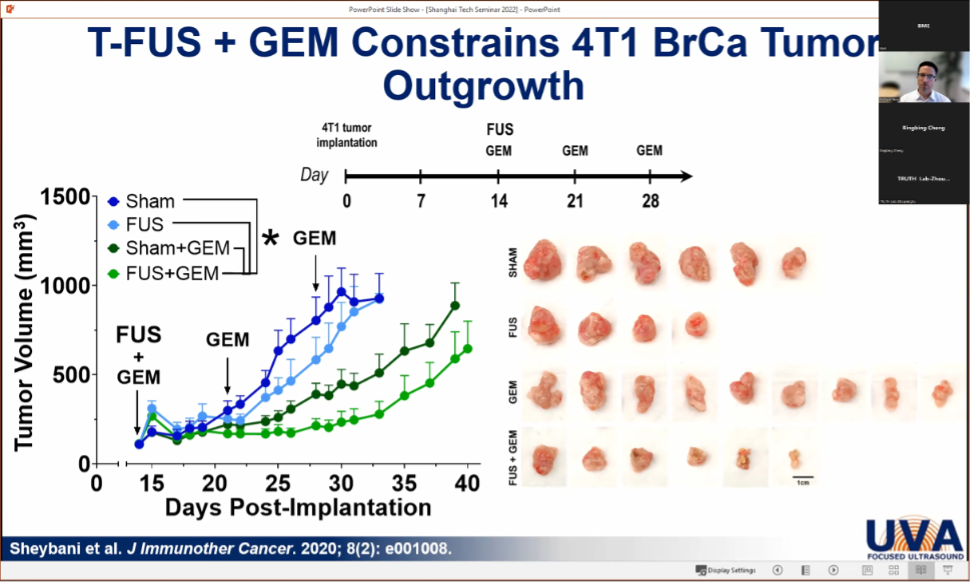
接着,他介绍了在小鼠上进行靶向热消融的实验仪器设备。该设备由超声成像探头、高强度聚焦超声 (HIFU) 换能器、三轴电机和实验受体支架等构成,能够可视化、实时地对靶点进行超声治疗。随后,他介绍了 T-FUS 在 4T1 乳腺癌上的应用,使用 T-FUS 结合吉西他滨 (GEM,治疗乳腺癌的化疗药物) 可以有效地限制原发性肿瘤生长,提高生存率并增强免疫原性。这种策略有望成为乳腺癌治疗的新选择,值得未来的临床评估。
T-FUS 与 GEM 结合抑制肿瘤生长
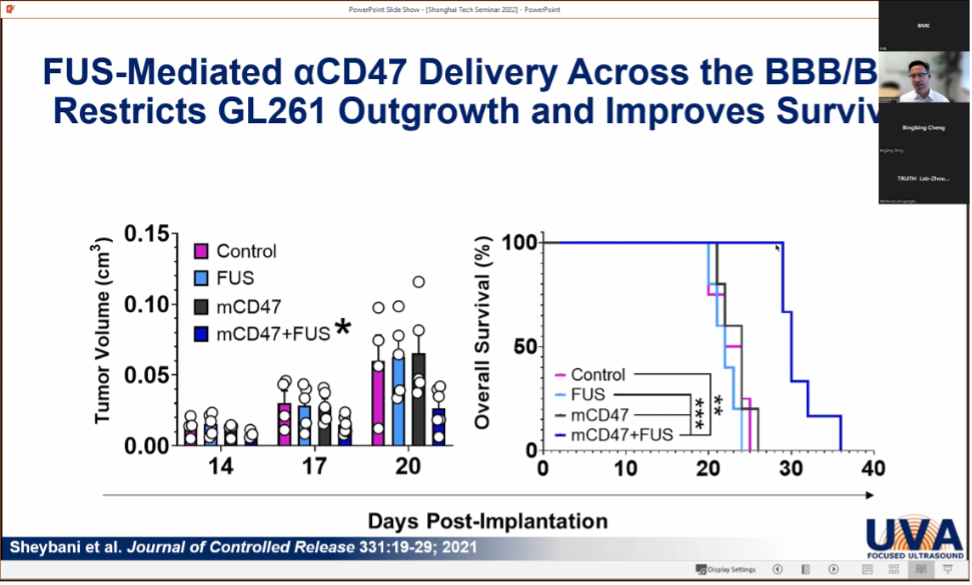
接着,Price 教授讲述到,FUS 结合微泡可以暂时地打开血脑屏障,从而打破血脑屏障阻碍药物分子进入脑内的禁锢,能将治疗性药物或基因递送至脑内。结合现今治疗胶质母细胞瘤的一个有潜力但受限于血脑屏障的方法——通过吞噬细胞阻断 CD47 进行癌症免疫治疗,发现 FUS 结合mCD47 (anti-mouse CD47 能够阻断 CD47) 可以显著抑制肿瘤生长,延长胶质瘤小鼠生存期。通过这一研究结果证实,使用 FUS 递送 mCD47 是治疗胶质母细胞瘤的一种有前途的治疗策略。
FUS 成功递送 mCD47 后脑肿瘤体积变化
及小鼠存活率图
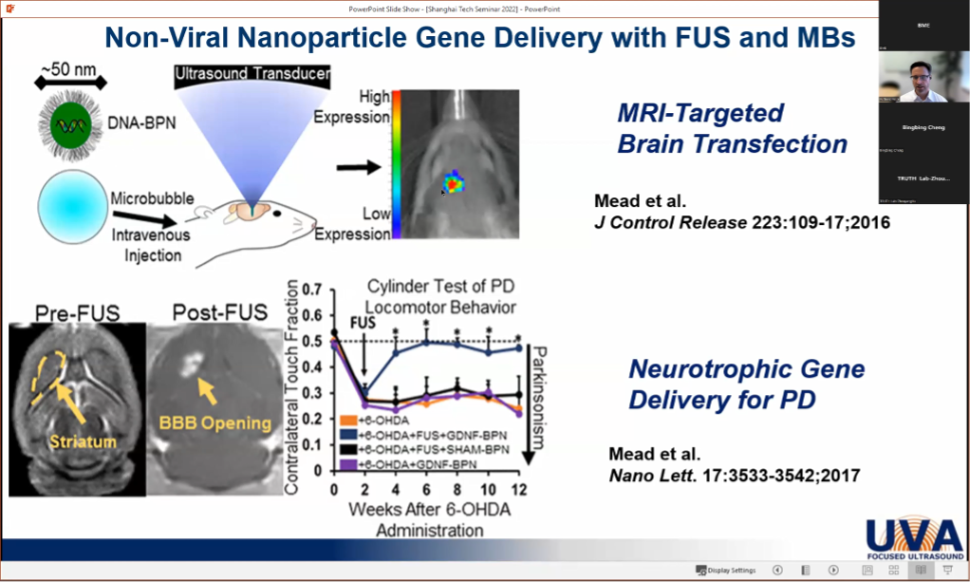
在 FUS 机械效应的应用中,Price 教授还介绍了其课题组在结合 FUS 和纳米材料进行药物递送方面的工作。如在 2016 年,他们通过实验证明,在图像引导下结合 FUS 和微泡进行携带 DNA 的脑穿透纳米颗粒 (DNA-BPN) 的递送是一种安全、无创的脑靶向基因治疗策略,这种策略有望治疗中枢神经系统的多种疾病,包括脑肿瘤和神经退行性疾病;在 2017 年,他们使用磁共振图像引导的FUS和GDNF-BPN (携带胶质细胞源性神经营养因子的脑穿透纳米颗粒) 结合的治疗方法,恢复了帕金森 (PD) 大鼠模型体内多巴胺水平和多巴胺能神经元密度,逆转了 PD 相关运动功能障碍的行为指标,并且没有出现局部或全身毒性,克服了当前药物递送方法的局限性,为治疗 PD 提供了一种新方法;在 2020 年 Price 课题组首次利用磁共振图像 (MRI) 引导的 FUS 结合微泡将 BPN 基因载体穿过脑肿瘤屏障/血脑屏障 (BTB/BBB) 递送到脑内并转染脑肿瘤,观察发现 FUS 辐照区域血脑屏障开放,并且肿瘤间质流量显著增加,证明了 FUS 对于增强 BPN 在肿瘤组织的转运中起着关键作用。
FUS 与微泡结合的非病毒纳米颗粒基因递送
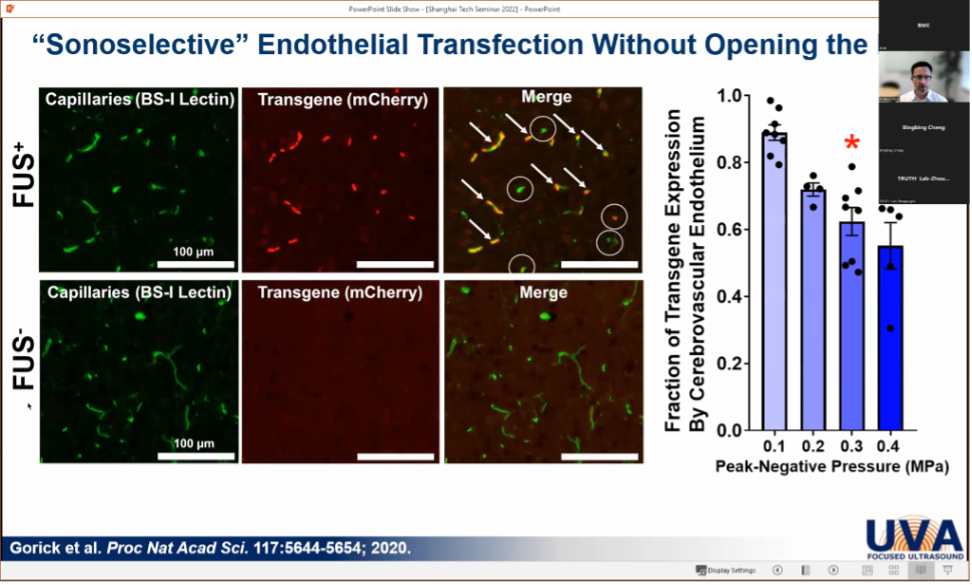
接下来 Price 教授介绍了另外一些 FUS 机械效应的应用,主要针对 FUS 在血脑屏障研究安全性上的三个注意点:1. 脑血管内皮细胞具有丰富的靶点;2. 内皮细胞特异性启动子反映弱且不稳定;3. 对于某些适应症 (如中风) ,任何血脑屏障的破坏都可能造成伤害。在这里,Price 教授介绍了一种 MR 图像引导下 FUS 治疗新方法,该方法能在不打开血脑屏障的情况下诱导脑血管系统的内皮选择性转染,即“声选择性”转染。通过大量的 RNA 测序表明,声选择性低压方案不会上调炎症或免疫反应;单细胞 RNA 测序表明声选择性转染的脑内皮细胞的转录组不受治疗的影响。这一方法允许靶向基因传递到血管,并可用于促进血管生成,释放内皮细胞分泌因子以刺激神经再生或补充神经干细胞。
FUS 在血脑屏障上的研究安全性的三个注意点
使用低压 FUS 策略在不打开血脑屏障的情况下进行内皮选择性转染
讲座最后 Price 教授介绍了 FUS 在脑海绵状血管畸形 (CCM) 中的应用。目前,手术切除是 CCM 唯一的治疗选择,并且临床上缺少针对性的药物手段。对此,他特别强调 FUS 对于脑海绵状血管畸形的治疗也具有非常广阔的前景。讲座末尾 Price 教授、程教授与众学者、观众进行了热烈的互动讨论。
本期讲座完整录像请关注“上科大生医工学院”官方哔哩哔哩账号观看,观看地址:
https://www.bilibili.com/video/BV1ut4y1V7Nq/